感染性骨缺損在臨床上非常常見,其致病菌主要為金黃色葡萄球菌[1]。交通事故和爆炸傷的增多使其發(fā)病率逐漸上升[2]。長(zhǎng)期靜脈應(yīng)用抗生素治療感染性骨缺損可導(dǎo)致身體毒性。載抗生素的聚甲基丙烯酸甲酯(polymethyl methacrylate,PMMA)已被廣泛用于治療骨感染性疾病[3]。PMMA的優(yōu)點(diǎn)是可在局部獲得較高的藥物濃度,避免了靜脈用藥的副作用;其主要缺點(diǎn)是不可降解、不能釋放全部藥物[4]。基于目前研究現(xiàn)狀,研發(fā)一種具有良好生物相容性、藥物緩釋性能、可控吸收、良好生物力學(xué)性能的骨修復(fù)材料對(duì)治療感染性骨缺損具有重要意義。
納米羥基磷灰石(nano-hydroxyapatite,n-HA)的結(jié)構(gòu)與人體骨組織相似[5],其具有良好的生物活性和相容性,n-HA被認(rèn)為是最有前途的骨修復(fù)材料之一[6]。n-HA負(fù)載萬(wàn)古霉素復(fù)合材料已成功用于治療感染性骨缺損[7]。聚氨酯(polyurethane,PU)是一種可生物降解的材料,已被廣泛用于骨組織工程[8]。納米羥基磷灰石/聚氨酯(n-HA/PU)多孔骨修復(fù)支架材料具有優(yōu)良的生物相容性和成骨作用。介孔二氧化硅納米粒子(mesoporous silica nanoparticles,MSNs)由Kresge等[9]首次發(fā)現(xiàn),具有大孔體積、可控孔徑、高比表面積等特點(diǎn),已被廣泛應(yīng)用于生物納米技術(shù)和納米醫(yī)學(xué)領(lǐng)域[10]。許多藥物和生物分子,如DNA或siRNA封裝在MSNs中用于治療癌癥[11]。左氧氟沙星是一種從氧氟沙星中分離出來(lái)的Ⅲ類氟喹諾酮類抗生素。其抗菌性能是氧氟沙星的2倍,具有低分子量,通過(guò)靜電吸引易于與MSNs結(jié)合。本研究以多孔n-HA/PU復(fù)合支架作為載體,將含有抗生素的MSNs分布于其多孔表面,合成了一種新型介孔硅納米微球載藥控釋抗菌骨修復(fù)材料,并評(píng)價(jià)該新型復(fù)合支架材料的體外緩釋性能及其治療感染性骨缺損的療效。
1.1 材料
24只新西蘭兔由菏澤醫(yī)學(xué)專科學(xué)校動(dòng)物實(shí)驗(yàn)中心提供,其中雌性12只,雄性12只,體重在2 ~ 4 kg之間,單籠飼養(yǎng)。動(dòng)物生產(chǎn)許可證號(hào):[SCXK(魯)-2018-0006],動(dòng)物使用許可證號(hào):[SYXK(魯)-2019-0019]。本實(shí)驗(yàn)研究經(jīng)菏澤醫(yī)學(xué)專科學(xué)校附屬醫(yī)院倫理委員會(huì)審核并通過(guò)(2021-016),并嚴(yán)格遵守“3R”原則。
蓖麻油、甘油、十六烷基三甲基溴化銨(CTAB)、原硅酸四乙酯(TEOS)(中國(guó)阿拉丁有限公司);1,4-丁二醇(BDO)和辛酸亞錫(中國(guó)成都科龍有限公司);左氧氟沙星、甲醛溶液、乙酸乙酯(中國(guó)國(guó)藥集團(tuán)化學(xué)試劑有限公司);聚甲基丙烯酸甲酯粉末(Palacos R+G,德國(guó)Heraeus Medical GmbH公司)。高效液相色譜儀(LC-2010AHT,日本島津公司);超聲波清洗器(KQ2200B,昆山市超聲儀器有限公司);高速離心機(jī)(D-37520,美國(guó)Sigma公司);循環(huán)恒溫水浴鍋(TB-85,日本島津公司);組織勻漿機(jī)(T10 basic S25,德國(guó)IKA公司);Micro CT掃描儀(μCT40,瑞士Scanco醫(yī)療);Scanco醫(yī)療系統(tǒng)(SC5073,μCTv6.1版,瑞士Scanco醫(yī)療);硬組織切磨系統(tǒng)(E300CP,德國(guó)EXAKT公司)。
1.2.5 植入材料
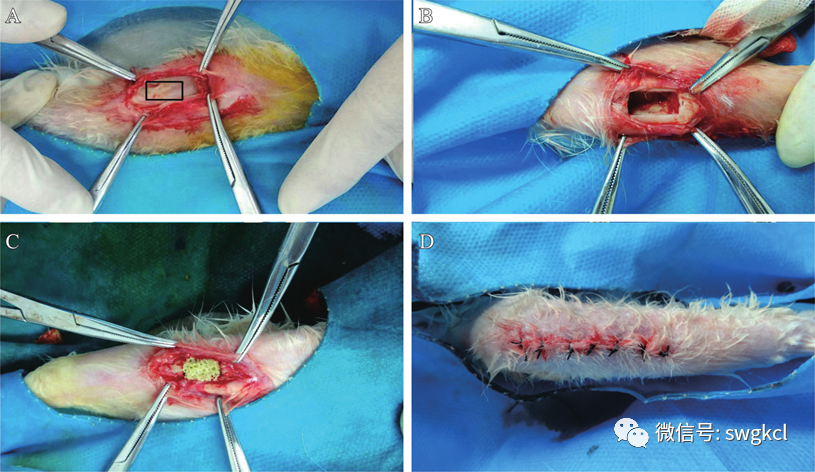
圖1 植入材料的過(guò)程:A. 暴露脛骨,選定清創(chuàng)區(qū)域與大小(10 mm×6 mm);B. 徹底清創(chuàng)并開窗;C. 植入復(fù)合支架材料;D. 逐層縫合
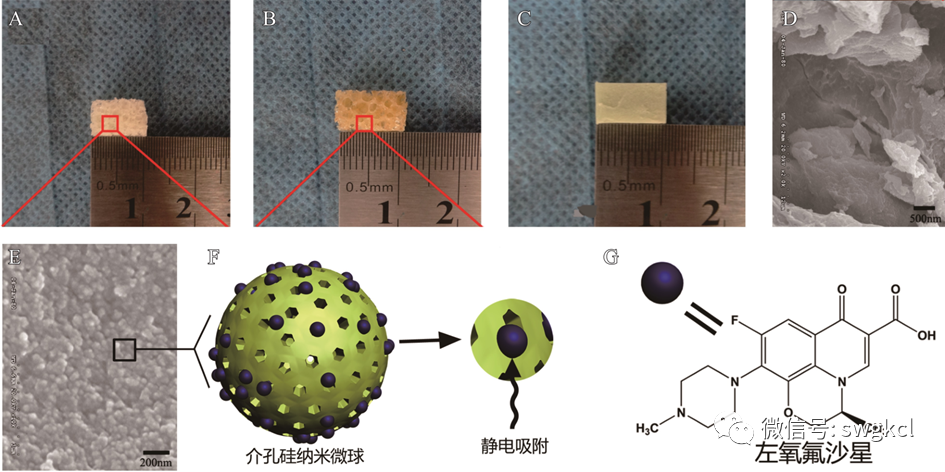
圖2 新合成的多孔復(fù)合支架材料:A. 空白n-HA/PU支架材料;B. 載抗生素后的n-HA/PU材料;C. 載抗生素的PMMA;D. 空白n-HA/PU的掃描電鏡圖;E. 1 mg Lev/n-HA/PU材料的掃描電鏡圖;F. 左氧氟沙星與MSNs結(jié)合的模式圖;G. 左氧氟沙星的分子結(jié)構(gòu)
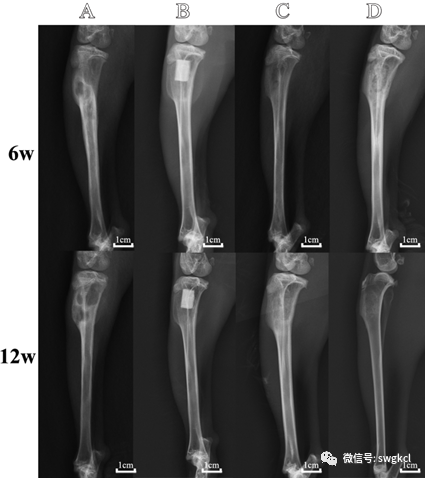

在植入后6周時(shí),單純清創(chuàng)組可見骨破壞和骨缺損。n-HA/PU組和1 mg Lev/n-HA/PU組的復(fù)合支架保持完整沒(méi)有降解。在n-HA/PU組和1 mg Lev/PMMA組中,可見支架材料周圍少量的新骨形成。在1 mg Lev/n-HA/PU組的支架周圍觀察到新的骨小梁形成。在植入后12周的時(shí)間點(diǎn),單純清創(chuàng)組表現(xiàn)為脛骨局部骨缺損,無(wú)明顯新生骨。在1 mg Lev/n-HA/PU組中,新生的骨小梁緊密地附著在復(fù)合支架上,幾乎填滿了整個(gè)骨髓腔。然而在n-HA/PU組和1 mg Lev/PMMA組中只能觀察到很少的新生骨小梁。各組植入后的3D重建如圖5所示。
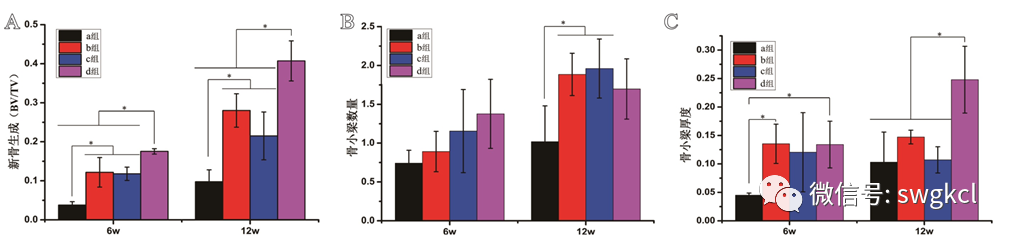
在植入后6周時(shí),1 mg Lev/n-HA/PU組的新骨生成量(BV/TV)均與其余三組有統(tǒng)計(jì)學(xué)差異(P<0.05)。在植入后12周時(shí),1 mg Lev/n-HA/PU組的新骨生成量(BV/TV)均高于其余三組(P<0.05,見圖6)。同時(shí),n-HA/PU組與1 mg Lev/PMMA組的新骨生成均高于單純清創(chuàng)組(P<0.05)。在植入后6周時(shí),各組之間新生骨小梁的數(shù)量比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。在植入后12周時(shí),n-HA/PU組與1 mg Lev/PMMA組的新生骨小梁的數(shù)量均高于單純清創(chuàng)組(P<0.05)。在植入后12周時(shí),1 mg Lev/n-HA/PU組的新生骨小梁的厚度均與其余三組差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。
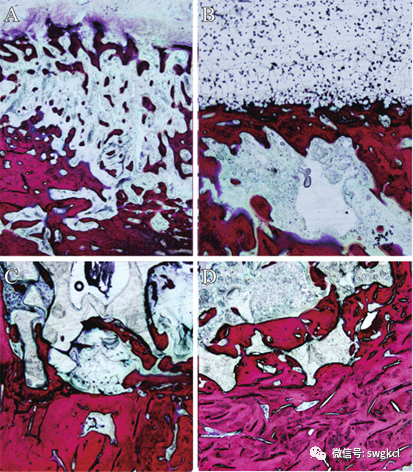
在植入后12周時(shí)由于炎癥反應(yīng)導(dǎo)致骨破壞,單純清創(chuàng)組骨質(zhì)較稀疏(見圖7A)。在1 mg Lev/PMMA組材料表面,可見明顯界限,有新生骨小梁遷延生長(zhǎng)(見圖7B)。在n-HA/PU組、1 mg Lev/n-HA/PU組材料的內(nèi)部,新生骨小梁沿孔隙生長(zhǎng)。其中1 mg Lev/n-HA/PU組材料與骨小梁相互纏繞,結(jié)合緊密(見圖7)。
感染性骨缺損的治療需徹底清除死骨和感染的軟組織,同時(shí)靜脈應(yīng)用抗生素4 ~ 6周[18]。其主要缺陷是局部的抗生素濃度達(dá)不到最小抗菌濃度,同時(shí)長(zhǎng)期靜脈應(yīng)用抗生素會(huì)對(duì)身體產(chǎn)生毒性,給患者帶來(lái)巨大的經(jīng)濟(jì)負(fù)擔(dān),對(duì)外科醫(yī)生來(lái)講是一個(gè)巨大的挑戰(zhàn)。因此,局部應(yīng)用抗生素治療感染性骨缺損成為了骨科學(xué)者研究的熱點(diǎn)。
本研究中,筆者將負(fù)載左氧氟沙星的MSNs與n-HA/PU相結(jié)合,合成了一種新型復(fù)合支架材料,用于治療感染性骨缺損。體外實(shí)驗(yàn)證實(shí)了其具有良好的藥物緩釋性能。將其植入動(dòng)物體內(nèi)12周后,新型復(fù)合支架材料具有良好生物相容性、抗感染能力、骨誘導(dǎo)能力,以期為感染性骨缺損的治療提供新的解決方案。
技術(shù)服務(wù)咨詢 步經(jīng)理 18910422384
 官方微信
官方微信艾佧科技(北京)有限公司 地址:北京市經(jīng)濟(jì)技術(shù)開發(fā)區(qū)地盛南街1號(hào)1幢3041室
2020@ 艾佧科技(北京)有限公司 京ICP備10236589號(hào)