目的 探究骨膜下植骨( Sub-periosteal Peri-implant Augmented Layer,SPAL) 技術(shù)對于修復(fù)種植體頰側(cè)骨缺損的組織學可靠性。方法 選取20只日本大耳白兔,應(yīng)用隨機數(shù)表法將其分為引導骨再生( Guided bone regeneration,GBR) 組(A組) 和SPAL組(B組) 兩組,每組各10只。拔除兔下頜切齒同期植入種植體建立骨缺損模型。骨增量 A 組采用 GBR技術(shù),B組采用 SPAL 技術(shù)。術(shù)后即刻、1個月、3個月、6個月取材進行 Micro CT 掃描及組織學觀察。結(jié)果 實驗操作可實現(xiàn)理想骨充填,術(shù)后 1個月時,B組種植體頰側(cè)多個水平層面骨壁厚度及整體骨體積均明顯高于A組。術(shù)后 3個月時,B組種植體頰側(cè)骨量高于A組,差異具有統(tǒng)計學意義( P<0.05) 。術(shù)后6個月時,兩組種植體頰側(cè)最終骨量趨于等量。組織學觀察可知,兩組種植體頰側(cè)均可實現(xiàn)成熟板層骨結(jié)構(gòu)。結(jié)論 SPAL 骨增量術(shù)后無纖維組織長入成骨區(qū),術(shù)后6個月可實現(xiàn)種植體骨結(jié)合及頰側(cè)骨再生,效果與傳統(tǒng) GBR技術(shù)無顯著差異。且骨膜替代人工屏障膜有利于維持原始骨壁,具有更好的空間維持作用。
【關(guān)鍵詞】 骨膜;屏障膜;骨再生;種植體
[中圖分類號]R78 [文獻標識碼]ADOI: 10.3969 /j.issn.1002-1256.2024.21.003
在臨床中,牙齒缺失后牙槽嵴頰側(cè)發(fā)生不同程度的水平向骨缺損的情況是非常常見的。這是由于隨著牙槽窩愈合過程中的骨改建和重塑[1],剩余牙槽嵴會發(fā)生一定程度的萎縮。其中,垂直向骨吸收通常為2~4 mm,且當鄰牙存在時吸收量更少,而水平向骨吸收可達 5~7 mm,相當于原牙槽嵴寬度的一半[2-3]。其中,頰側(cè)骨板吸收量又要遠遠多于舌側(cè)。
種植修復(fù)的目的在于恢復(fù)口腔功能及美學效果; 保證遠期的穩(wěn)定; 減少并發(fā)癥風險。其中,保證遠期穩(wěn)定性的關(guān)鍵在于要確保種植體全部位于健康的牙槽骨內(nèi),且骨壁厚度至少 1.5 mm[4-6]。當種植體頰側(cè)骨壁存在裂開型骨缺損時,發(fā)生種植體周圍炎的風險會大大提高[7-8],且軟組織并發(fā)癥增多。當種植體頰側(cè)骨壁完整但厚度<1.5 mm 時,術(shù)后2個月該位點會發(fā)生約3mm 的垂直向骨吸收; 而當頰側(cè)骨壁
厚度>1.5 mm 時,遠期骨量基本保持穩(wěn)定[9]。綜上所述,無論是種植體頰側(cè)存在骨缺損還是頰側(cè)骨壁完整但厚度<1.5 mm,都必須進行骨增量手術(shù)恢復(fù)頰側(cè)骨壁厚度。
GBR技術(shù)是目前口腔種植臨床中最常用的骨增量術(shù)式[10]。GBR的原理就是通過屏障膜的應(yīng)用阻止缺損區(qū)內(nèi)增殖較快的上皮細胞和成纖維細胞長入,從而保證增殖速度較慢的成骨細胞和血管能夠優(yōu)先長入屏障膜下方血凝塊占據(jù)的間隙內(nèi)[11]。但由于 GBR術(shù)中的骨膜減張切口破壞了骨膜結(jié)構(gòu)的完整性,損傷了骨膜生發(fā)層,使得骨膜的成骨潛能在 GBR術(shù)式未能得到充分利用。
SPAL是一種種植同期修復(fù)頰側(cè)骨缺損的新型術(shù)式[12]。通過對頰側(cè)瓣進行半厚分離,外層黏膜瓣可達到無張力的冠向復(fù)位,實現(xiàn)傷口的嚴密關(guān)閉。內(nèi)層完整的骨膜瓣不僅降低了手術(shù)創(chuàng)傷,同時為骨膜成骨潛能的發(fā)揮奠定了解剖學基礎(chǔ)。由于避免了人工屏障膜的使用,手術(shù)成本大大降低。在Trombelli 的臨床研究中確實報道了理想的成骨效果。但目前SPAL 技術(shù)缺乏對種植體周骨水平的長期追蹤,成骨質(zhì)量以及骨再生過程中是否有纖維組織長入不得而知。本研究欲通過動物實驗,探究 SPAL 技術(shù)對于修復(fù)種植體頰側(cè)骨缺損的組織學可靠性。
1.實驗動物: 選取20只日本大耳白兔,雄性,1~2 歲齡,平均體重 2.5~3.0kg,口腔內(nèi)無疾患。應(yīng)用隨機數(shù)字表法將其分為 GBR 組( A 組) 和 SPAL 組( B 組) 兩組,每組各10只,每只兔下頜可提供2個實驗位點。
2.設(shè)備和材料: (1) 鈦合金種植體3.5mm×8mm及配套覆蓋螺絲; (2) 骨增量材料 Gesitlich Bio-Oss,Gesitlich Bio-Gide; (3) 常規(guī)手術(shù)器械; (4) 打磨機;(5) 小動物顯微 CT( Micro CT,Bruker Skyscan1276) ;(6) EXAKT 300PC 硬組織切片機( 德國 EXAKT公司) ; (7) EXAKT 400 磨片機( 德國 EXAKT 公司) ;(8) 研磨砂紙( 320、800、1200、4000目,德國) ; (9) 生物顯微鏡( 奧林巴斯 BX53) 。
3.研究方法: (1) 手術(shù)方式: ①術(shù)前準備: 實驗前3天確認實驗動物身體精神狀況良好,可以承受外科手術(shù)操作。對實驗動物進行稱重,按照300mg /kg 應(yīng)用全麻藥物。肌內(nèi)注射全麻藥物鹽酸賽拉嗪注射液后,等待3~5min,若動物仍與麻醉前活躍程度相似,則再次給予異氟烷吸入性麻醉藥物,增強麻醉效果2~3min 后,可見動物活躍度明顯降低。使用棉絮輕輕觸及動物眼瞼緣,檢查動物眼瞼反射消失,同時觀察到瞳孔縮小,拉動動物四肢無肌張力后,表明實驗動物已進入手術(shù)麻醉狀態(tài)。將實驗動物仰臥,四肢用繃帶纏繞固定于兔臺上,使用棉簽蘸取碘伏消毒液充分擦拭動物口腔內(nèi)部及上下唇,鋪無菌孔巾。②翻瓣及微創(chuàng)拔牙: 于實驗動物下頜兩顆切齒的頰側(cè)齦頰溝處再次局部注射阿替卡因腎上腺素注射液行浸潤麻醉,1~2min 后,使用15c刀片做下頜切齒的齦溝內(nèi)切口,切斷下頜正中系帶與牙面的附著。刀片盡量與牙體長軸平行,避免損傷骨膜組織。再在兩顆切齒遠中做水平附加切口,長度約2mm,如圖 1A。小心剝離頰側(cè)黏膜直至暴露頰側(cè)牙槽嵴,保證骨膜組織完整,如圖1B。適當剝離舌側(cè)黏膜,同樣注意保證骨膜完整。翻瓣完成后,開始微創(chuàng)拔牙。使用刃薄的骨膜分離器置于兩顆切齒之間的牙槽間隔處,近遠中向施力挺松牙齒,如圖 1C。止血鉗加持牙齒后小幅度頰舌向、近遠中向晃動,并向上、向內(nèi)旋轉(zhuǎn)施力拔出切齒,如圖1D。此時可見拔牙窩舌側(cè)骨壁高聳,頰側(cè)骨壁的高度低于舌側(cè)約3~5mm。頰側(cè)骨壁表面存在天然滋養(yǎng)孔結(jié)構(gòu),孔內(nèi)可見紅色血液。使用咬骨鉗少量去除舌側(cè)高聳骨壁,使頰舌側(cè)骨壁的高度差約為2mm,如圖1E。注射器抽取氯化鈉注射液后沖洗拔牙窩并使用無菌紗布擦干。③植入種植體及骨增量: 于拔牙窩內(nèi)手動旋入實驗用種植體,至種植體平臺水平高于頰側(cè)牙槽嵴頂約2mm,即種植體頰側(cè)冠方2mm 處暴露在骨壁之外,舌側(cè)完全位于骨壁內(nèi),如圖1F~H。實驗組的骨增量操作:首先,使用兩把鑷子分別加持頰側(cè)黏骨膜瓣的近遠中冠方邊緣,稍微用力提起黏骨膜瓣可形成口袋狀。將 Bio-Oss 小顆粒骨移植材料用氯化鈉注射液浸濕后覆蓋于種植體頰側(cè),并嚴密充滿頰側(cè)黏骨膜瓣所形成的口袋,如圖 1I。再將頰側(cè)黏骨膜瓣與舌側(cè)瓣拉攏對位縫合。對照組的骨增量操作為: 先根據(jù)兩顆切齒頰側(cè)骨壁的尺寸和形狀修剪 Bio-Gide 可吸收生物膠原膜,保證長度足夠覆蓋牙槽嵴頂及舌側(cè)。使用15c刀片輕輕劃斷頰側(cè)黏骨膜瓣偏根方的骨膜組織,避免割斷全層組織,此時可見少量出血,如圖1J。將修剪合適的生物膠原膜插入口袋狀的黏骨膜瓣內(nèi)側(cè),血液浸透膠原膜根方,使其與黏骨膜瓣的根方貼合,冠方仍保持干燥直立,如圖1K。同樣Bio-Oss小顆粒骨移植材料用氯化鈉注射液浸濕后覆蓋于種植體頰側(cè),并嚴密充滿頰側(cè)黏骨膜瓣所形成的口袋,如圖 1L。此時將生物膠原膜向舌側(cè)反折,完全覆蓋牙槽嵴頂后插入到舌側(cè)黏骨膜瓣內(nèi),再使用氯化鈉注射液潤濕,使之貼合,如圖 1M。將頰側(cè)黏骨膜瓣與舌側(cè)瓣拉攏對位縫合,如圖 1N。④術(shù)后取材: 術(shù)后連續(xù)3d肌內(nèi)注射抗生素,預(yù)防術(shù)后感染。進行正常喂養(yǎng),創(chuàng)口縫線不拆除,任其自行脫落。術(shù)后即刻 A、B組各處死一只兔進行下頜前部取材,術(shù)后 1個月、3個月、6個月 A、B 組各處死三只取材。(2) Micro CT 掃描測量: 標本進行 Micro CT 掃描,使用CTAn分析軟件測 量: ①種植體頰側(cè)骨壁厚度(Buccal bone thickness,BBT) ,分別選取種植體頂端水平(BBT1) 、頂端根方2mm(BBT2) 、頂端根方4mm(BBT3) 及頂端根方6mm(BBT4) 水平測量種植體頰側(cè)骨壁厚度; ②種植體頰側(cè)骨壁體積(buccal bone volume,BBV) 。(3) 組織學觀察: 標本經(jīng)脫水包埋后,沿頰舌向縱向切割為200μm切片,依次研磨至20~30μm,然后進行 Leva-Laczko 染色過程,形成最終切片,進行觀察。
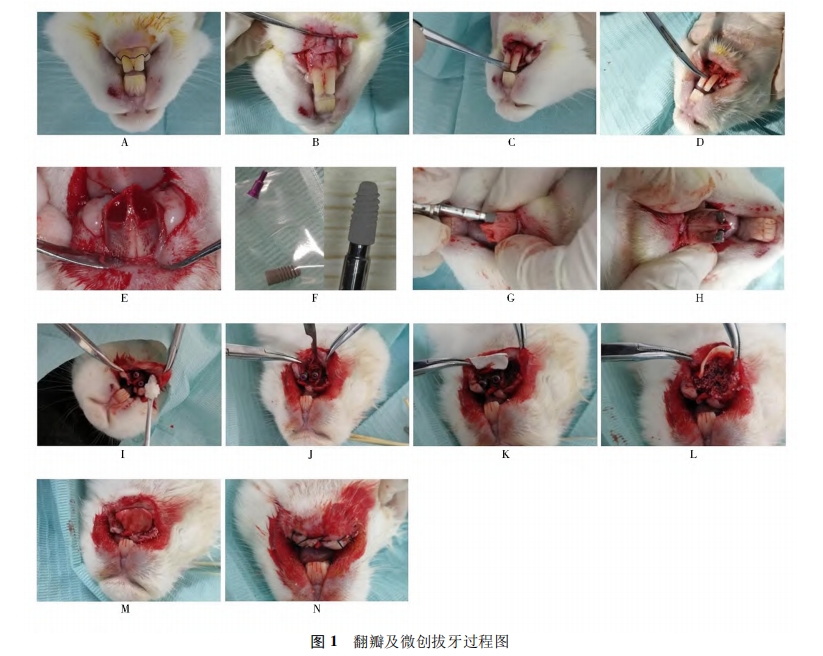
所有實驗動物術(shù)后一般狀況良好,無死亡,口腔內(nèi)創(chuàng)口無感染、裂開,無種植體、顆粒狀骨移植材料、生物膠原膜暴露。



技術(shù)服務(wù)咨詢 步經(jīng)理 18910422384
 官方微信
官方微信艾佧科技(北京)有限公司 地址:北京市經(jīng)濟技術(shù)開發(fā)區(qū)地盛南街1號1幢3041室
2020@ 艾佧科技(北京)有限公司 京ICP備10236589號